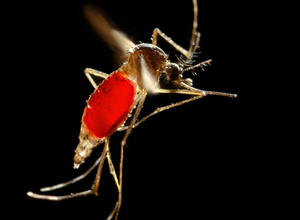
Blockierte Fortpflanzung: Mit Gentechnik gegen unerwünschte Insekten
Zahlreiche Insekten übertragen Krankheitserreger oder schädigen Nutzpflanzen. 2014 wurden in Brasilien erstmals gentechnisch veränderte Tigermücken mit einem „selbstlimitierenden“ Gen zugelassen, um Infektionen durch das Dengue- und Zika-Virus einzudämmen. Im Mai 2024 wurden in Afrika gv-Anopheles-Mücken freigelassen, um die Übertragung von Malaria zu verhindern. Den Ansatz des selbstlimitierenden Gens verfolgt man auch bei Pflanzenschädlingen. Seit April 2021 ist in Brasilien der Einsatz gentechnisch veränderter Heerwürmer erlaubt, um die Schädlingspopulation in Schach zu halten.
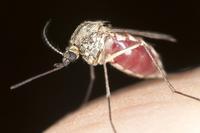
Stechmücken übertragen verschiedene Infektionskrankheiten wie Dengue-Fieber, Malaria und Zika. Mit dem Klimawandel ist ihr Vorkommen längst nicht mehr auf die Tropen beschränkt.

Die Kohlmotte (Plutella xylostella) verursacht weltweit immense Schäden, vor allem bei Kohlgewächsen. In den USA wurden gv-Motten mit selbstlimitierendem Gen bereits im Freiland getestet.
Fotos: iStockphoto, Oxitec; großes Foto oben: James Gathany / CDC
Stechmücken sind die gefährlichsten Tiere der Welt: Sie übertragen die Erreger für einige der schlimmsten Infektionskrankheiten des Menschen, die oft tödlich verlaufen. Weltweit erkranken jedes Jahr rund 200 Millionen Menschen an Malaria, eine halbe Million Menschen sterben daran. Beim Dengue-Fieber sind es jährlich 50-100 Millionen Erkrankungen und 20.000 Todesfälle.
In der Landwirtschaft sorgen Insekten für zum Teil erhebliche Ernteausfälle, entweder durch direkte Fraßschäden oder durch die Übertragung von Pflanzenkrankheiten. Zahlreiche Nutzpflanzen werden deswegen regelmäßig mit Insektiziden behandelt.
Aufgrund des weltweiten Reise- und Warenverkehrs werden heute immer wieder krankheitsübertragende Insekten und landwirtschaftliche Schädlinge eingeschleppt. Durch die steigenden Temperaturen in Folge des Klimawandels können sie - oft aus tropischen und subtropischen Gebieten stammend - auch hierzulande überleben. Die Asiatische Tigermücke (Aedes albopictus) etwa ist immer häufiger auch in Deutschland anzutreffen, im Südwesten haben sich bereits feste Populationen etabliert. Asiatische Tigermücken können mehr als 20 zum Teil gefährliche Viren übertragen, etwa Dengue-, Zika-, Chikungunya- oder West-Nil-Viren.
Auch landwirtschaftliche Schadinsekten breiten sich bei uns immer weiter nach Norden aus, so die aus Südostasien stammende Kirschessigfliege (Drosophila suzukii), die im Obstbau große Schäden verursacht. Zukünftig werden effektive Bekämpfungsmaßnahmen gegen solche krankheitsübertragenden Insekten und landwirtschaftlichen Schädlinge auch hierzulande immer wichtiger werden.
Ein Ansatz zur Eindämmung unerwünschter Insekten ist, ihre Fortpflanzung zu verhindern. Einige Forschungsprojekte setzen dabei auch gentechnische Methoden ein. Am weitesten fortgeschritten sind die Entwicklungen der britischen Firma Oxitec, einer Ausgründung der University of Oxford. Das Unternehmen nutzt ein sogenanntes „selbstlimitierendes“ Gen, das in das Erbgut männlicher Insekten eingeführt wird. Bereits 2014 wurden erstmals gentechnisch veränderten (gv) Ägyptischen Tigermücken (Aedes aegypti) in Brasilien für die kommerzielle Nutzung genehmigt. Bei den gv-Mücken (OX513A) führt die genetische Veränderung dazu, dass der Nachwuchs schon im Larvenstadium stirbt. Seit der Zulassung wurden in Brasilien in mehreren Städten gv-Mücken freigelassen. In den betroffenen Stadtbezirken gingen die Mückenpopulationen um mehr als 80 Prozent zurück und entsprechend auch die Zahl der Infektionen in der Bevölkerung.
Inzwischen wurden die gv-Tigermücken so weiterentwickelt (2. Generation, OX50340), dass nur der weibliche Nachwuchs stirbt (nur die Weibchen stechen und übertragen Krankheitserreger). Die männlichen Mücken tragen das „selbstlimitierende“ Gen in die nächste Generation weiter. Da das Gen an jeweils die Hälfte der Nachkommen weitergegeben wird, verbleibt es länger in der Mückenpopulation, nimmt aber mit der Zeit ab. Gv-Mücken der zweiten Generation wurden im Mai 2020 in Brasilien zugelassen.
In einem Pilotprojekt in Florida wurden 2021 an verschiedenen Standorten 144.000 gv-Tigermücken über mehrere Monate freigesetzt. Erste Ergebnisse zeigten, dass die gv-Insekten sich wie geplant verhielten und das „selbstlimitierende“ Gen in der Population zwei bis drei Monate bzw. drei Generationen überdauerte. 2022 genehmigte die zuständige US-Behörde weitere Freisetzungen in Florida und Kalifornien.
Zusammen mit der Bill & Melinda Gates-Stiftung arbeitet Oxitec daran, die Technologie auch bei verschiedenen Anopheles-Mückenarten anzuwenden. Bei Anopheles stephensi ist die Entwicklung bereits so weit, dass im Mai 2024 in Djibouti und damit erstmals in Ostafrika gv-Mücken dieser Art freigelassen wurden. A. stephensi - ursprünglich aus Asien stammend - breitet sich besonders in den Städten rasant aus und überträgt Malaria. Eine Bekämpfung ist mit den herkömmlichen Methoden schwierig, da die Mücken tagsüber stechen und Mosquitonetze somit nicht helfen. Außerdem haben sich bei A. stephensi bereits Resistenzen gegen die üblichen Insektizide entwickelt.
Nicht nur Oxitec, sondern auch eine Reihe von Projekten an Forschungsinstituten beschäftigt sich damit, die Übertragung von Infektionskrankheiten durch Insekten mit Hilfe gentechnischer Methoden einzudämmen. Unter dem Dach von Target Malaria, einem gemeinnützigen Forschungsverbund, wurden zum Beispiel im Juli 2019 erstmals gv-Anopheles gambiae-Mücken in Burkina Faso freigesetzt, bei denen die Männchen durch Gentechnik steril gemacht wurden. Die Ergebnisse dieser Freisetzung sind positiv und entsprechen den Erwartungen.
Heute werden neben den klassischen Gentechnik-Methoden auch zunehmend die neuen Genome Editing-Verfahren angewandt, um Insektenpopulationen einzudämmem. Mit Hilfe der Gen-Schere CRISPR/Cas konnten beispielsweise Wissenschaftler in den USA und in Großbritannien zeigen, dass die gezielte Veränderung bestimmter Gene dazu führt, dass weibliche Mücken ihre Flugfähigkeit verlieren, die sie für Nahrungsaufnahme und Fortpflanzung brauchen.
In einigen Projekten wird daran gearbeitet, mit CRISPR/Cas die veränderten Merkmale mit einem Gene drive zu kombinieren. Dieser sorgt dafür, dass sich die neuen Erbinformationen in den jeweiligen Populationen schnell von selbst verbreiten. Die Notwendigkeit einer wiederholten Freilassung von gv-Mücken könnte damit umgangen werden. Da mit Gene drive eine Art theoretisch vollständig ausgelöscht werden könnte, wird die Methode sehr kritisch gesehen. Eine Expertengruppe beschäftigt sich daher damit, besondere Leitlinien für die Risikobewertung und das Management von Gene drive-Organismen zu erarbeiten. Eine Freisetzung ist bisher weltweit noch in keinem Land genehmigt worden.
„Sterblichkeitsgen“ auch bei Pflanzenschädlingen
Bisher werden Schadinsekten an landwirtschaftlichen Nutzpflanzen vorwiegend mit Insektiziden bekämpft. Deren Einsatz ist aber umstritten, da die Mittel oft nicht spezifisch genug wirken und auch nützliche Insekten abtöten können. Den Ansatz mit einem „selbstlimitierenden“ Gen verfolgt die Firma Oxitec deshalb auch bei Pflanzenschädlingen. So hat Oxitec bereits Kohlmotten, Mittelmeer- und Olivenfruchtfliegen, Kirschessigfliegen, Baumwollkapselwürmer, Sojabohnenschleifer und Herbst-Heerwürmer mit einem „Sterblichkeitsgen“ ausgestattet. In Brasilien wurden im April 2021 erstmals gv-Herbst-Heerwürmer (Spodoptera frugiperda) für den Einsatz in der Landwirtschaft zugelassen. Die Larven treten oft massenweise auf und verursachen große Schäden, vor allem an Mais. Der Kleinschmetterling stammt ursprünglich aus Amerika und breitet sich seit 2016 auch in Afrika und Südostasien aus, wo er die Maisernte der Kleinbauern bedroht.
Die Kohlmotte (Plutella xylostella) verursacht weltweit vor allem bei Kohlgewächsen immense Schäden. Schon 2017 wurden gv-Kohlmotten in den USA im Freiland getestet. Erste Ergebnisse deuten darauf hin, dass der Einsatz der gv-Motten eine wirksame Schädlingsbekämpfung ermöglichen könnte.
Nach zahlreichen Versuchen in geschlossenen Glashäusern in Australien, Griechenland und Marokko sind auch Freilandversuche mit gv-Mittelmeerfruchtfliegen (Ceratitis capitata) geplant. Die Fruchtfliege befällt eine Reihe an Kulturpflanzen, vor allem Zitrusfrüchte, aber auch Mangos, Feigen, Kaffee und Pfirsiche. Die Larven entwickeln sich im Fruchtfleisch und zerstören es dadurch. Zudem sind die Bohrlöcher Eintrittspforten für sekundäre Schaderreger wie Pilze und Bakterien.
Auch mehrere Forschungsinstitute arbeiten daran, Schadinsekten mit Hilfe von Gentechnik oder Genome Editing einzudämmen. Die meisten Projekte befinden sich noch im Bereich der Grundlagenforschung. Erfolgreiche Anwendungen beschränken sich bisher noch auf relativ wenige Insektengruppen (u. a. Motten, Fliegen, Heuschrecken). Das liegt vor allem daran, dass der Einsatz von Genome Editing technische Schwierigkeiten mit sich bringt: Das bei Tieren übliche Einbringen der molekularen Scheren in die Eier durch Mikroinjektion ist sehr kompliziert. Aber auch hier kommt die Forschung voran. Bei einigen Arten konnte bereits geklärt werden, ob und wie ein Eingriff mit CRISPR/Cas überhaupt möglich ist, z.B. bei der Olivenfruchtfliege (Bactrocera oleae) und bei der Tabakmottenschildlaus (Bemisia tabaci).
Gentechnik und Genome Editing: Weitere Projekte mit Insekten (Beispiele)
| Insektenart | Ziel | Verfahren | Wer | Stand |
|---|---|---|---|---|
| Anopheles-Mücke (Anopheles gambiae) | sterile Weibchen | CRISPR/Cas | Imperial College London, UK | L |
| Anopheles-Mücke (A. gambiae) | geringerer Befall mit Malariaerregern, geringere Fitness | CRISPR/Cas | Johns Hopkins University, USA | L |
| Ägyptische Tigermücke (Aedes aegypti) | Weibchen entwickeln sich zu Männchen | Gentechnik | Virginia Tech, USA | L |
| Asiatische Tigermücke (Ae. albopictus) | Weibchen entwickeln sich zu Männchen | CRISPR/Cas | Southern Medical University, China | L |
| Ägyptische Tigermücke (Ae. aegypti) | Keine Verbreitung von Dengue-Viren | Gentechnik | University of California, USA | L |
| Kohlmotte (Plutella xylostella) | weiblicher Nachwuchs stirbt | Gentechnik | Oxitec, UK | F, USA |
| Kirschessig-Fliege (Drosophila suzukii) | weiblicher Nachwuchs stirbt | Gentechnik | Oxitec, UK | E |
| Sojabohnen-Schleifer (Chrysodeixis includens) | weiblicher Nachwuchs stirbt | Gentechnik | Oxitec, UK | E |
L = Labortests, F = Freilandversuche, E = frühe Entwicklungsphase
Diskussion / Kommentare
 Kommentare werden geladen…
Kommentare werden geladen…
Themen

Moskitos sind die mit Abstand tödlichsten Tiere der Welt. Auf ihr Konto gehen mehr Todesopfer als auf alle anderen Tiere, den Menschen eingeschlossen. (Our World in Data)
Wie wir einen unserer tödlichsten Feinde vernichten können - Gene Drive & Malaria (Kurz gesagt -In a nutshell)
Project to Control Disease-Carrying Mosquitoes Kicks Off in the Florida Keys (Oxitec)
Im Web
- Djibouti Breaks New Ground in the Fight Against Malaria with First Release of Friendly Mosquitoes in Africa, Targeting the Invasive Anopheles stephensi. Oxitec, 23.05.2024
- First results from US trial of genetically modified mosquitoes. Nature 604 (28.04.2022)
- Oxitec - Friendly & Powerful technology for a changing planet
- Brazil approves environmentally ‘Friendly’ GM tool for controlling fall armyworm. Cornell Alliance for Science (15.04.2021)
- Shelton A.M. et al. (2020): First Field Release of a Genetically Engineered, Self-Limiting Agricultural Pest Insect: Evaluating Its Potential for Future Crop Protection. Frontiers in Bioengineering and Biotechnology
- O’Leary, S. & Adelman, Z.N. (2020): CRISPR/Cas9 knockout of female-biased genes AeAct-4 or myo-fem in Ae. aegypti results in a flightless phenotype in female, but not male mosquitoes. PLoS Negl. Trop. Dis. 14(12)
- Streit um Milliarden Gentech-Insekten, Kathrin Zinkant, SZ (21.09.2019)
- „Fucking irresponsible“ – Gentechnik und Medien, Ludger Wess, Salonkolumnisten (21.09.2019)
- Results of the small-scale release of non gene drive genetically modified sterile male mosquitoes in Burkina Faso. Target Malaria, Okt. 2022