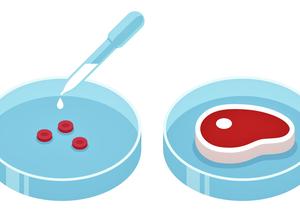
Echtes Fleisch aus Zellkultur: Ohne Tierhaltung, aber mit viel High-Biotech
Kein Ersatz aus Pflanzen, sondern „echtes“ Fleisch, aber aus kultivierten Zellen, ohne dafür Tiere halten und schlachten zu müssen: Vor wenigen Jahren war das noch eine ferne Utopie. Inzwischen gibt es außerhalb Europas erste Produkte zu kaufen. Auch in der EU sind bereits Zulassungsanträge eingereicht, etwa vom Kulturfleisch-Pionier Mosa Meat aus Maastricht. Die Kosten für die Produkte sinken drastisch, die Qualität wird immer besser. Und bei den so wichtigen Kulturmedien gibt es endlich „tierfreie“ Alternativen zu den anfangs verwendeten Kälberseren. Der Schlüssel dazu sind moderne, leistungsfähige Bio- und Labortechnologien – Gentechnik eingeschlossen. Doch der Weg bis zu einer relevanten Alternative zum klassischen Fleisch scheint schwieriger als gedacht.

Mark Post, Professor an der Universität Maastricht und Gründer von Mosa Meat präsentiert den ersten Hamburger aus Fleisch, das in Zellkulturen „vermehrt“ worden war (2013).

So lecker und appetitlich wie vom Tier: Zielgruppe für Zellkulturfleisch sind nicht Vegetarier wie bei Fleischimitaten auf Pflanzenbasis, sondern überzeugte Fleischesser.
Fotos: Mosa Meat; großes Foto oben: iStock/Liudmila Chernetska
Der erste Rindfleisch-Burger, der „im Labor“ aus sich vermehrenden Muskelzellen herangewachsen war, kostete noch 250.000 Euro. Mark Post, Physiologie-Professor an der Universität Maastricht (NL), hatte viele Jahre darauf hingearbeitet. Als er ihn 2013 öffentlich verkostete, wollte Post auf großer Bühne zeigen, dass sich „echtes“, schmackhaftes Fleisch in Zellkulturen erzeugen lässt, ohne dafür Tiere halten und schlachten zu müssen. Etwa zehn Jahre werde es dauern, bis eine Massenproduktion möglich sei, meinte Post damals.
Inzwischen gibt es außerhalb Europas erste Produkte zu kaufen, doch eine ernsthafte Konkurrenz zu „richtigem“ Fleisch sind sie aktuell noch nicht. Ganz daneben lag Post mit seiner optimistischen Prognose zwar nicht, doch die technologischen Hürden, gutes Zellkultur-Fleisch in gewohnter Qualität in großen Mengen zu produzieren, scheinen höher als anfangs gedacht.
Trotz aller Herausforderungen hat sich in den letzten Jahren eine ganze Branche entwickelt. Das Good Food Institute (GFI), ein „gemeinnütziger Think Tank, der sich dafür einsetzt, das globale Ernährungssystem für den Planeten, die Menschen und die Tiere zu verbessern“, listet in seiner Datenbank aktuell 168 Unternehmen auf allen Kontinenten auf, die sich mit der Entwicklung von kultiviertem Fleisch und Meeresprodukten beschäftigen. Hinzu kommen 27 „aktive“ Produktionsstätten sowie 17 weitere, die sich gerade im Aufbau befinden (September 2025).
Inzwischen sind es nicht mehr allein kleine, kreative Startups, welche die Entwicklung vorantreiben, sondern auch etablierte Player aus der Fleisch- oder Pharmabranche. So investiert etwa die PHW-Gruppe, eine der größten Geflügelproduzenten Europas, zu der auch Wiesenhof gehört, 40 Millionen Euro in eine strategische Partnerschaft mit dem von Mark Post gegründeten niederländischen Branchenpionier Mosa Meat (April 2024). Bei einer anschließenden Crowd Fonding-Kampagne sammelte Mosa Meat innerhalb weniger Minuten mehr als 1,5 Mio Euro von 800 Kleinanlegern.
Von der Zelle zum Fleischstück
Gleich ob Rind, Lamm, Huhn oder Fisch – um In vitro-Fleisch zu erzeugen, gehen alle ähnlich vor: Mittels Biopsie werden den Tieren, bestimmte Stammzellen entnommen, etwa aus der Skelettmuskulatur oder aus dem Bindegewebe. Daraus werden stabile, gut charakterisierte Zelllinien gewonnen, deren Zellen sich immer weiter vermehren und in verschiedene Typen ausdifferenzieren, etwa Muskel-, Fett und Bindegewebe.
Damit größere Fleischstücke in einer charakteristischen Form und Textur entstehen, ist eine Gerüststruktur erforderlich, ganz ähnlich wie im natürlichen Tier. Geeignete Gerüste zu entwickeln, an die sich die kultivierten Zellen anlagern und ein komplexes Fleischprodukt wie Steak oder Hühnchenbrust entsteht, ist der „heilige Gral der kultivierten Fleischindustrie“ (Good Food Institute). Mit den aktuellen Techniken könne dieses „Kunststück“ noch nicht vollbracht werden. Deswegen gehen die Zellkultur-Pioniere erst einmal mit technisch weniger anspruchsvollen Burger-Patties, Nuggets oder Hackfleisch auf den Markt. Bis ein gutes, bezahlbares „echtes“ Rindersteak „aus dem Labor“ auf den Markt kommt, wird es wohl noch etwas dauern.
Damit sich die Fleischzellen in der Kultur immer wieder teilen und dabei zu verschiedenen Zelltypen ausdifferenzieren, sind geeignete Kulturmedien nötig. Sie liefern essentielle Nährstoffe, etwa Glukose, Salze, Vitamine und Aminosäuren, aber auch Komponenten, die für die Erhaltung und Vermehrung der Zellen benötigt werden, etwa spezielle Proteine, Wachstumsfaktoren, Hormone oder Lipide – ein hochkomplexes Gemisch. Lange Zeit war man dafür auf Rinderserum (FBS) angewiesen, das aus dem Blut ungeborener Kälber gewonnen wird. Ein „wunderbarer Saft, mit dem wir fast alles machen können“, schwärmt ein Entwickler, doch er ist nicht nur extrem teuer, sondern mit den eigenen hohen moralischen Ansprüchen kaum vereinbar.
Zellwachstum: Die biotechnischen Alternativen zum Rinderserum
Etwa 400 bis 800 Euro kostet ein Liter Kälberserum, bis zu 50 Liter wurden anfangs davon für einen Beef Burger benötigt. 55 bis 95 Prozent der Kosten für Zellkulturfleisch entfallen auf die Nährmedien, schätzt das Merck Innovation Center. Billigere und vor allem tier-freie Seren sind nicht nur der Schlüssel für eine Massenproduktion, sondern auch für eine breite öffentliche Akzeptanz.
Die Zellfleisch-Startups, aber auch erfahrene Biotech-Unternehmen arbeiten mit Hochdruck an alternativen tierfreien Kulturmedien. Welche Technologien sie dabei einsetzen und wie weit sie dabei sind, verraten sie in der Regel nicht. Vor allem Proteine und verschiedene Wachstumsfaktoren, Schlüsselsubstanzen für die Zellen in den Bioreaktoren, können nur mit Hilfe bio- und gentechnischer Verfahren hergestellt werden. Albumin, ein Blutplasmaprotein, das etwa Nährstoffe und Hormone transportiert, ist das mit Abstand das mengenmäßig wichtigste Protein für Zellkulturfleisch. Der künftige Bedarf – „Millionen Kilogramm jährlich“ (GFI) – kann nur über die Produktion mit gentechnisch veränderten Mikroorganismen gedeckt werden.
Auf der Suche nach tierfreien Zellmedien hat man in Pflanzen oder Algen Wachstumsfaktoren und Proteine entdeckt, welche die Teilung der kultivierten Muskelzellen anregen. Meist sind die natürlich vorkommenden Konzentrationen dieser Substanzen jedoch extrem gering. Der Weg, „um solche Stoffe in großen Mengen und zu bezahlbaren Kosten herzustellen, ist die Biotechnologie“, so Post. Mit den Konzepten der Synthetischen Biologie können Stoffwechselwege in Mikroorganismen „eingebaut“ werden, damit sie die benötigten Stoffe ohne Mengenbegrenzung produzieren (siehe auch: Präzisionsfermentation).
ORF Genetics, ein junges isländisches Biotech-Unternehmen, will die begehrten Wachstumsfaktoren aus Pflanzen gewinnen und dafür Erfahrungen nutzen, die es bei der Produktion von ähnlichen Wirkstoffen für Kosmetika und Anti-Aging-Produkte gewonnen hat – hergestellt in gentechnisch veränderter Gerste (Molecular Farming), die in großen abgeschlossenen Gewächshäusern angebaut wird. Inzwischen bietet das Unternehmen eine ganze Palette „tierähnlicher“ Wachstumsfaktoren für Rinder-, Schweine- und Hühner-Kulturfleisch an (Markenname Mesokine).
Einen Schritt weiter scheint Mosa Meat zu sein. Schon 2019 hatte das Unternehmen erklärt, es könne „vollständig auf fötales Rinderserum und andere tierische Komponenten verzichten“ und zugleich die Kosten für Zellkultur-Fleisch um das 80-fache senken – ohne jedoch genauer darzulegen, wie es dieses für die Zukunft der Branche so wichtige Ziel erreicht wurde. Inzwischen hat Mosa Meat sein patentiertes Verfahren in einem wissenschaftlichen Artikel in Natur Food vorgestellt (Januar 2022).
Ein Forscherteam des Unternehmens hatte sich auf molekularer Ebene den Prozess näher angeschaut, in dem die Ausgangszellen zu verschiedenen Muskelzellen differenzieren. „Wir haben uns besonders für Proteine auf der Oberfläche von Zellen interessiert, die während der Differenzierung zunehmen“, so Tobias Messmer, Erstautor und Doktorand. Diese Proteine – auch als „Rezeptoren“ bezeichnet – werden nun durch genau für diesen Zweck designte Stoffe aktiviert. Dadurch „sind wir in der Lage, den gleichen Übergang in Abwesenheit von FBS-Rinderserum nachzubilden.“
Der Erfolg von Mosa Meat zeigt auch, was heute mit modernen, hochentwickelten Labor- und Analyseverfahren – unterstützt durch künstliche Intelligenz bei der Auswertung riesiger Datenmengen – möglich ist: Wenn man auf molekularer Ebene ermittelt hat, was Zellen in einer bestimmten Phase für Wachstum und Differenzierung benötigen, können Hunderte von Komponenten systematisch darauf untersucht werden, ob sie diese Anforderungen erfüllen. Auf Basis dieser Daten lässt sich dann ein optimales Medium „entwerfen“, das – biotechnologisch hergestellt – den gleichen Zweck erfüllt wie bisher die Rinderseren.

Produktion von kultiviertem Hähnchenfleisch. Pilotanlage von GOOD Meat (USA). Foto: GOOD Meat
Zulassung, Kosten, Umweltbilanzen - der lange Weg zum Markterfolg
Doch bis Fleisch aus Zellkultur tatsächlich einen nennenswerten Teil des aktuellen Fleischkonsums ersetzt, ist es noch ein langer Weg. Das erste, zunächst nur begrenzt erhältliche Produkt waren Chicken Nuggets und andere geformte Hühnchenstücke. Nach zweijähriger Prüfung waren sie 2020 in Singapur zugelassen worden.
Im März 2023 folgte die US-Lebensmittelbehörde FDA. Sie bestätigte dem Hersteller GOOD Meat, alle Fragen zur Sicherheit seien geklärt und der Verzehr unbedenklich. Ein paar Monate später kam auch die Zulassung der Landwirtschaftsbehörde USDA. In vitro-Hühnchen-Fleisch – ebenso wie das des Konkurrenten Upside Foods – darf in den USA nun hergestellt und frei vermarktet werden. Beide Unternehmen kündigten an, ihr Lab-grown Chicken zunächst in einzelnen renommierten Restaurants anbieten zu wollen. Derzeit werden ambitionierte Produktionskapazitäten aufgebaut. Doch so rasch und problemlos wie die Unternehmen es darstellen, läuft es offenbar nicht. Das Scaling up, das Herauffahren der Biorekatoren auf große Mengen, scheint schwieriger als anfangs gedacht.
Mehrere Länder – Kanada, Australien, Israel und auch die Europäische Union – haben vor Jahren besondere gesetzliche Vorschriften für „neuartige Lebensmittel“ (Novel Food) eingeführt, unter die auch die neuen „tierfreien“ Fleischprodukte aus Zellkultur fallen. So dürfen in Europa solche Produkte nur dann auf den Markt, wenn die Hersteller deren Sicherheit und Verträglichkeit auf Basis wissenschaftlicher Daten zweifelsfrei haben nachweisen können – eine hohe Hürde. Zudem dürfen die Verbraucher nicht getäuscht werden. Schon jetzt wird darum gestritten, ob Laborfleisch an der Ladentheke als „Fleisch“ deklariert werden darf.
Bis die ersten Produkte in der EU tatsächlich zu kaufen sind, wird es noch einige Zeit dauern, auch wenn inzwischen erste Zulassungsanträge eingereicht sind: Den Anfang machte Foie Gras, eine traditionelle, vor allem in Frankreich geschätzte Pastete aus Entenleber, für die jedoch keine jungen Enten mehr qualvoll gemästet werden müssen. Gestellt hatte ihn das Unternehmen Gourmay, das unterstützt von der französischen Regierung seit längerem an einer tierfreien Alternative gearbeitet hatte.
Im Januar 2025 reichte der Kulturfleisch-Pionier Mosa Meat ein umfangreiches Antragsdossier für kultiviertes Rinderfett ein, eine Schlüsselkomponente. „Indem wir unser kultiviertes Rinderfett zur Zulassung einreichen, unternehmen wir einen der letzten Schritte zur Einführung unserer innovativen Produkte – wie dem Mosa Burger – auf dem europäischen Markt.“ Anders als in USA oder Singapur müssen in der EU alle Zutaten für Kulturfleisch-Produkte einzeln zugelassen werden. Nach der Vorprüfung durch die Europäische Kommission folgt die wissenschaftliche Sicherheitsbewertung durch die Europäische Lebensmittelbehörde EFSA. Sie wird mindestens 18 Monate dauern. Auch für die Schweiz und Großbritannien hat Mosa Meat einen ähnlichen Antrag gestellt. (Übersicht Zulassungen weltweit: siehe Tabelle unten)
Im niederländischen Maastricht hat Mosa Meat ein neues Entwicklungszentrum mit einer großen Scaling up-Produktionsanlage in Betrieb genommen. Das, so Mosa Meat-Chef Marten Bosch „macht uns zum weltweit größten Campus für kultiviertes Fleisch und bietet eine solide Grundlage für unsere europäischen und globalen Vermarktungspläne.“ Anfang Juli 2023 erlaubte die niederländische Regierung eine begrenzte Verkostung von Zellkultur-Fleisch unter „kontrollierten Bedingungen“ – noch vor einer offiziellen Zulassung. Politisch strittig war das nicht. Eine Mehrheit im Parlament und fast alle dort vertreten Parteien hatten zugestimmt.
In Großbritannien ist seit Februar 2025 Futter für Hunde und andere fleischfressende Haustiere auf dem Markt, ohne „echtes“ Fleisch, sondern aus kultivierten Hühnchenzellen. Die britischen Behörden hatten das weltweit erste Produkt dieser Art im August 2024 zugelassen.
Inzwischen beschäftigen sich erste Studien mit Stoffströmen, Energie- und Umweltbilanzen. Nach einer 2023 publizierten LCA-Studie (Life Circle Assessment) ist der Landverbrauch bei kultiviertem Fleisch deutlich geringer als bei der Tierhaltung. Auch fallen weniger Stickstoff-bedingte Emissionen an, da keine Gülle entsteht. Allerdings ist der Energieverbrauch von Kulturfleisch hoch. Nur, wenn erneuerbare Energien genutzt werden, ist der CO2-Fußabdruck bei Rind und Schwein geringer als der bei Fleisch aus traditioneller Landwirtschaft, bei Huhn ist er für beide ähnlich hoch.
Allerdings spielen bei der Akzeptanz noch andere Dinge eine Rolle als Umwelt und Sicherheitsbewertungen. Vielen erscheint das „grüne“ Fleisch aus dem Bioreaktor als Angriff auf die traditionelle Fleischkultur und die damit verbundene Lebensweise. Einige US-Bundestaaten – Florida, Alabama, Mississippi, Nebraska – haben bereits ein Verbot von Kulturfleisch beschlossen mit drastischen Strafen für Verstöße dagegen. Damit soll die traditionelle landwirtschaftliche Fleischerzeugung gegen die „leblosen“ High-Tech-Alternativen aus dem Labor geschützt werden. Auch Italien hat Zellkulturfleisch weit vor möglichen EU-Zulassungen erst einmal verboten.
Produkte aus Zellkultur-Fleisch: Zulassungen und Zulassungsanträge weltweit (Stand: September 2025)
| Fleischprodukt aus Zellkultur | EU | Andere Länder | ||
| Foi Gras (Entenleber) Gourmey |
Antrag auf Zulassung als Novel Food (Aug 2024) | Anträge in UK, Schweiz, USA, Singapur | ||
| Hot Dogs aus Zellkultur mit Pflanzenproteinen The Cultivated B |
Zulassungsantrag in der Vorprüfung | |||
| Rindfleisch Mosa Meat, Meatable |
Erlaubnis für Verkostung unter kontrollierten Bedingungen (Niederlande) | |||
| Rinderfett (Komponente für kultiviertes Fleisch) Mosa Meat |
Antrag auf Zulassung nach Novel Food für kuliviertes Rinderfett (Jan 2025) | Antrag in der Schweiz (März 2025) und in UK (Mai 2025) | ||
| Heimtierfutter auf Basis von Hühnchenfleisch Meatly |
Zugelassen in UK (Aug 2024); Vermarktung ab Feb 2025 | |||
| Angus-Rindfleisch Aleph Farms |
Zugelassen in Israel (Jan 2024), Zulassungsanträge in UK und Schweiz (Kooperation Migros) | |||
| Hühnchenfleisch Upside Foods, Good Meat |
Zugelassen in den USA (Jun 2023) und Singapur (2020) | |||
| Wachtelfleisch Vow, (Markenname: Forged) |
Zugelassen in Australien und Neuseeland (Juni 2025) | |||
| Lachs (kultiviert, kombiniert mit pflanzlichen Zutaten) Wildtype |
Zugelassen in den USA (Juni 2025) | |||
| Kultiviertes Schweinefett Mission Barns |
Zugelassen in den USA (Juli 2025) |
Diskussion / Kommentare
 Kommentare werden geladen…
Kommentare werden geladen…
Themen
Noch unbezahlbar. Mark Post präsentiert den ersten Hamburger aus Zellkultur-Fleisch. (London, August 2013)
In-vitro-Fleisch: Eine Alternative (Quarks)
Der Laborfischer – Sebastian Rakers kultiviert zellbasierten Fisch im Bioreaktor (Die Biopioniere, Bioökonomie.de)
Im Web
- Good Food Institute, Culivated Meat
- Good Food Institute Europe
- Nature Food, October 2022; Focus on cellular agriculture
- Emily Waltz, Club-goers take first bites of lab-made chicken; Nature 10 March 2021
- In-vitro-Fleisch oder -Fisch: Welche Produkte sind wo bereits erlaubt? Top Agrar
- Mosa Meet
- Mosa Meat, Submitting Our First EU Market Authorisation Request; 22 Jan 2025
- MosaMeat Conducts First Pre-Approval Tasting of Cultivated Beef in the EU; 25 July 2024
- Mosa Meat, Cultivation beef without FBS; 13. Jan 2022
- T. Messmer et al, A serum-free media formulation for cultured meat production supports bovine satellite cell differentiation in the absence of serum starvation; Nature Food, 13. Jan 2022
- GOOD Meat (Eat Just Inc.)
- GOOD Meat Gets Full Approval in the U.S. for Cultivated Meat (21. Jun 2023)
- Upside Foods (früher: Memphis Meats)
- UPSIDE is approved for sale in the US! Here’s what you need to know. 21. Jun 2023
- ORF Genetics, Animal-like growth factors for the cell cultured meat market (Mesokine)
- Pelle Sinke et al; Ex-ante life cycle assessment of commercial-scale cultivated meat production in 2030; Lca for Energy Systems and Food Products (2023)
- EU-Commission: Novel Food