Klimaresiliente Pflanzen: Was bringt die Gen-Schere CRISPR/Cas?
Von Juliette Irmer
Das Jahr 2024 war das wärmste seit Beginn der globalen Temperaturaufzeichnung. Die Folgen der Klimaerwärmung sind weltweit spürbar: Dürren, Waldbrände, Starkregen und Überschwemmungen werden häufiger und führen zu teils erheblichen Ernteeinbußen. Um langfristig ausreichend Nahrungsmittel zu produzieren, braucht es robuste Nutzpflanzen, die dem Klimawandel trotzen. Den neuen Genome Editing-Verfahren, vor allem der Gen-Schere CRISPR/Cas, kommt dabei eine Schüsselrolle zu. Was damit möglich ist, zeichnet sich inzwischen deutlicher ab.
Die Klimaentwicklung der vergangenen Jahre lässt erahnen, was die Zukunft bereithält: Ein insgesamt unbeständigeres Wetter mit Dürren, späten Frösten, Dauerregen oder Hitzeperioden. Die Landwirtschaft stellt das vor besondere Herausforderungen, denn viele Nutzpflanzen können sich nur eingeschränkt anpassen. Global betrachtet bedeutet das Ernteeinbußen - wirtschaftliche Verluste in reichen Ländern, Hunger in armen Regionen der Erde.
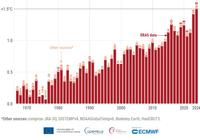
Globale Temperaturen: Jährlicher Anstieg gegenüber dem vorindustriellen Zeitalter (1850-1900). Era5-Daten: Copernicus-Projekt der EU; andere Daten aus anderen internationalen Beobachtungssystemen. Daten: C3S/ECMWF
Großes Foto oben: iStock
Höhere Temperaturen setzen Pflanzen auf vielfältige Art unter Stress: Hitze beeinträchtigt ihren Stoffwechsel und ihr Wachstum, ebenso wie Trockenheit und ein höherer Salzgehalt im Boden. Derart geschwächte Pflanzen haben auch Schädlingen und Krankheiten wenig entgegenzusetzen, was die Situation zusätzlich verschärft.
Ein Grad wärmer: 10 Prozent weniger Erträge allein bei Weizen und Mais
Sorgen bereitet Experten vor allem mögliche Ernterückgänge bei den drei Getreidesorten Weizen, Reis und Mais, die wichtigsten Grundnahrungsmittel. Zusammen liefern sie über die Hälfte der Kalorien, die die Weltbevölkerung über pflanzliche Nahrung aufnimmt. Modelle schätzen, dass bereits ein Grad Temperaturanstieg die Weizen- und Maiserträge um bis zu 10 Prozent verringern könnte. Laut IPCC (Intergovernmental Panel on Climate Change) sind bei einer zusätzlichen Erwärmung über zwei Grad weltweit starke negative Effekte auf die Getreideproduktion sehr wahrscheinlich, was die Ernährungssicherheit gefährden würde. Sicher ist, dass auch andere Nutzpflanzen leiden, da auch Sojabohnen, Kartoffeln, Tomaten oder Kaffee, um nur einige zu nennen, hitze- und trockenheitsempfindlich sind.
Hinzu kommt, dass global betrachtet immer mehr Menschen auf abnehmenden Anbauflächen ernährt werden müssen, weil die Klimaerwärmung auch zur Landdegradierung beiträgt, etwa in Form von Bodenerosion. Vor diesem Hintergrund wird deutlich, dass es robuste Nutzpflanzen braucht, die verlässlich hohe Erträge liefern, also auch bei Hitze, Trockenheit und einem hohen Salzgehalt im Boden gut gedeihen und zusätzlich Krankheiten und Schädlinge abwehren können.
Um solche ertragreichen und zugleich widerstandsfähigen Nutzpflanzen zu züchten, kommen alle heute zur Verfügung stehenden Methoden zum Einsatz, also Kreuzungs- und Mutationszüchtung, klassische Gentechnik und auch Genome Editing. Den modernen Züchtungstechniken (NGT) kommt dabei eine Schlüsselrolle zu, denn sie erlauben eine im Vergleich zu konventionellen Zuchtmethoden schnellere Anpassung der Pflanzen: Genome Editing, insbesondere CRISPR/Cas, erlaubt erstmals punktgenaue kleine und größere Eingriffe in das Erbgut. Züchter brauchen sich nicht mehr auf den Zufall zu verlassen, sondern können Veränderungen gezielt ausschließlich in interessanten Genregionen vornehmen. Obendrein können Gene adressiert werden, die man mit Kreuzungen nicht erreicht: Bei gekoppelt vererbten Genen können etwa jene mit ungünstigen Eigenschaften ausgeschalten werden
Das Interesse an den neuen Züchtungstechniken ist enorm, wie eine Datenbankanalyse dokumentiert: Die Zahl der Fachveröffentlichungen im Zusammenhang mit CRISPR/Cas9-Anwendungen zur Verbesserung der Stresstoleranz und des Ertrags von Nutzpflanzen, insbesondere von Reis, Weizen und Mais, hat zwischen 2019 und 2025 deutlich zugenommen.
Die Forschungsergebnisse sind teils beachtlich und in einigen großen Agrarnationen wurden Crispr-editierte Pflanzen bereits zugelassen:
- Indien: Anfang Mai 2025 wurde der Anbau von zwei gen-editierten Reissorten zugelassen. Die beiden Sorten liefern einen höheren Ertrag und sind unempfindlicher gegenüber Trockenheit und Salzstress.
- China: Anfang 2025 hat das zuständige chinesische Ministerium fünf gen-editierte Pflanzensorten für die kommerzielle Nutzung zugelassen, darunter eine gegen Mehltau resistente Weizensorte. China ist der größte Weizenproduzent und -verbraucher der Welt.
- Brasilien: Der Anbau dürretolerante Sojabohnen wurde zugelassen, die Vermarktung ist für die Ernte 2027/28 geplant.
- USA: Gen-editierten Pflanzen mit verbesserten Eigenschaften wie nicht bräunende Avocados, Bananen und Pilze wurden bereits zugelassen. An mehltau-resistenten Weintrauben, salztolerantem Reis, hitzeresistentem Weizen und Soja wird geforscht.
Weniger anfällig gegen Pflanzenkrankheiten
Wissenschaftler erwarten im Zusammenhang mit der Erderwärmung auch ein verändertes Spektrum an Pflanzenkrankheiten und -schädlingen. Entsprechend häufig wird CRISPR/Cas genutzt, um Resistenzen gegen pathogene Viren, Bakterien und Pilze zu erzeugen: Etwa Reis, der gegen Bakterienbrand resistent ist, Bananen gegen BXW (Bananen Xanthomonas-Welke), Kartoffeln, die widerstandsfähiger sind gegen Kartoffelfäule (Phytophthora), eine weltweit gefürchtete Pilzerkrankung, Cassava (Maniok), mit einer besseren Abwehr gegen CMD (Cassava Mosaic Virus), eine Viruserkrankung, die für hohe Ernteverluste in Afrika und Asien verantwortlich ist. Auch Weizen, Mais, Kakao, Raps, Tomaten, Gurken und Weintrauben sollen mithilfe der Gen-Schere robuster gegen bestimmte Krankheiten werden.
Grundsätzlich ist es einfacher Nutzpflanzen gegen sogenannte biotische Stressfaktoren wie Krankheiten und Schädlinge zu wappnen, als ihre Toleranz gegenüber abiotischen Stressoren wie Hitze oder Salzgehalt zu erhöhen. Denn die Resistenz gegenüber Krankheitserregern beruht oft auf einzelnen Genen, die direkt an der Abwehr von Insekten, Pilzen oder Viren beteiligt sind. Oft reicht es, sie mithilfe der Gen-Schere auszuschalten, um die Widerstandskraft zu erhöhen. Selbst Pflanzen mit sehr komplexen Genomen, also 4, -6- oder sogar 8-fachem Chromosomensatz, etwa hexaploider Weizen oder oktoploide Erdbeeren, können mithilfe der Gen-Schere erfolgreich verändert werden.
Pflanzeneigenschaften wie Trockenheits- oder Salztoleranz sind hingegen hochkomplex: Sie werden in der Regel nicht durch einzelne Gene, sondern durch ein ganzes Netzwerk an Genen reguliert. Häufig sind verschiedene Transkriptionsfaktoren beteiligt, die in mehreren Stoffwechselwegen eine Rolle spielen. Schaltet man einen solchen Transkriptionsfaktor aus, ist das selten zielführend, weil man sich meist andere Probleme in Form unerwünschter Eigenschaften einhandelt. Bei derart komplexen Merkmalen stößt auch die CRISPR-Technologie immer wieder an ihre Grenzen. Sie hilft allerdings dabei, das Wissen über Gen-Funktionen und Gen-Netzwerke und generell über die komplexen Pflanzengenome, die oft um ein Vielfaches größer sind als das menschliche Genom, zu erweitern und zu beschleunigen: Indem etwa Mutationsreihen in Schlüsselgenen durchgeführt werden und beobachtet wird, wie sich die einzelnen Mutationen auf die Pflanze und ihr Wachstum auswirken.
So setzen Forscher die Gen-Schere mittlerweile auch im Promotor-Bereich ein, also der regulierenden Region, die auf dem DNA-Strang vor dem eigentlichen Gen liegt. Steuert man diesen Bereich mit der Gen-Schere an, wird das Gen nicht einfach ausgeschaltet, sondern es fällt zum Beispiel einer von mehreren Transkriptionsfaktoren aus, weil die Bindestelle verändert wurde. Dadurch wird das Gen etwa hoch- oder herunterreguliert, also mehr oder weniger Protein hergestellt, und man erhält zum Beispiel Unterschiede in der Größe oder der Anzahl der Früchte oder auch in der Trockenheitstoleranz.
Auf diese Art und Weise wurde etwa eine Maispflanze erzeugt, die Trockenheit besser toleriert. Dazu wurde der Promotor des Gens ARGOS8 so verändert, dass er fortlaufend aktiv ist, das Gen also permanent abgelesen wird.
Bei einer der klimaangepassten, indischen Reissorte wurde das DST-Gen (Drought Salt Tolerance) nicht komplett ausgeschaltet, sondern durch eine Deletion verändert: Die Reispflanzen verlieren dadurch weniger Wasser über die Spaltöffnungen (Stomata) und können so besser mit Salz- und Dürrestress umgehen.
Robuste Wildpflanzen in Kulturpflanzen umwandeln
Um die Trockenheits- oder Salztoleranz von Nutzpflanzen zu verbessern, kann man auch auf Wildpflanzen zurückgreifen: Viele von ihnen wurden niemals domestiziert, obwohl sie das Potenzial als Nutzpflanze hätten. „Hochgezüchtete Kulturarten, die ihre genetische Variabilität weitgehend verloren haben, hitzeresistent zu machen, ist ein schwieriges Unterfangen. Stattdessen sollten wir uns Pflanzen anschauen, die schon hitzeresistent sind und sie mithilfe von CRISPR/Cas in ertragreiche Kulturarten umwandeln“, erklärt Holger Puchta vom Karlsruher Institut für Technologie. So ist mittlerweile ein großer Teil der Schlüsselmutationen, die zu größeren Früchten und einem hohen Ertrag geführt haben, bekannt.
Mehrere Forschergruppen arbeiten bereits daran, den Ertrag sogenannter Orphan crops, also Nutzpflanzen, die auf dem Weltmarkt und in der Wissenschaft eine eher untergeordnete Rolle spielen, mithilfe von CRISPR/Cas zu erhöhen. Dazu gehören etwa Maniok, Hirse oder Teff, ein nahrhaftes und widerstandsfähiges Getreide aus Äthiopien. Im Idealfall würden Orphan crops oder Wildpflanzen mithilfe der Gen-Schere innerhalb von Jahren statt Jahrzehnten zu ertragreichen Kulturpflanzen, deren natürlichen Resistenzen gegen biotische und abiotische Faktoren bewahrt wurden.
Genome Editing ist kein Wunderwerkzeug, das alle Hürden der Pflanzenzucht beseitigen kann. Aber ein Werkzeug, das ständig verbessert wird: Zu den jüngsten Fortschritten gehören Prime Editing, Base Editing und Multiplexing-Techniken für noch präzisere und komplexere genetische Veränderungen. Durch künstliche Intelligenz können Off-target-Effekte weiter reduziert werden und auch bei einer der größten technischen Hürden, das Einbringen der Gen-Schere in die Pflanzenzelle, werden Fortschritte erzielt.
Weiterhin problematisch ist das Fehlen eines weltweit einheitlichen Rechtsrahmens. Die unterschiedlichen Regularien beeinträchtigen nicht nur den Anbau und die Vermarktung gen-editierter Produkte, sondern auch die Forschung.
| Vergleich von Mutationsraten: | ||
| Die natürliche Mutationsrate in Pflanzen variiert in Abhängigkeit der Umweltbedingungen wird aber auf etwa eine Mutation pro 150 Millionen Basenpaaren (Mbp) geschätzt. Das heißt, zwei Reispflanzen (Genomgröße 430Mbp) unterscheiden sich im Durchschnitt in etwa 3 Mutationen, zwei Weizenpflanzen (Genomgröße 16 Milliarden Bp) in rund 100 Mutationen. | ||
| Die klassische Mutagenese durch Strahlung oder Chemikalien erhöht die Mutationsrate etwa um das 1000fache. Hier findet man also etwa alle 100 000 bis 250 000 Basenpaare eine Mutation. Das macht bei Reis mit seinem kleinen Genom rund 2000 bis 4300 Mutationen aus, bei Weizen mit seinem Riesengenom zwischen 60 000 und 160 000 Mutationen aus. | ||
| Wie oft es bei der gerichteten Mutagenese mit CRISPR-Cas zu Fehlschnitten (off-targets), also Mutationen kommt, hängt entscheidend von der guideRNA ab. Meist wird die 20 Basen lange Sequenz so gewählt, dass sie sich an vier oder mehr Stellen von anderen Sequenzen im Genom unterscheidet, so dass ungewollte Schnitte nur sehr selten vorkommen. Bei Weizen sind das etwa 5 bis 6 Mutationen, bei kleineren Genomen entsprechend weniger. |
Diskussion / Kommentare
 Kommentare werden geladen…
Kommentare werden geladen…
Themen
Vorteil CRISPR/Cas. Robert Hoffie entwickelt am IPK Gatersleben Gerste mit einer Resistenz gegen eine Viruskrankheit. Ohne die Gen-Schere wäre das nicht möglich. (Reihe Die Biopioniere, bioökonomie.de)
Im Web
- R.L. Chavhan et al, Emerging applications of gene editing technologies for the development of climate-resilient crops; Front. Genome Ed., 10 March 2025
- Navjot Kaur et al, CRISPR/Cas9: a sustainable technology to enhance climate resilience in major Staple Crops; Front. Genome Ed., 18 March 2025
- Katyayni Kanth et al, Editing the Future: CRISPR/Cas9 for Climate-Resilient Crops; Research Gate
- Deepak K. Ray et al, Climate change has likely already affected global food production: PlosOne May 31, 2019
- Karen Massel, et al,; Hotter, drier, CRISPR: the latest edit on climate change. Theoretical and Applied Genetics, 134, 2021
- China approves more GM crops to boost yields, ensure food security; Reuters, Dec 31, 2024
- Subhra Priyadarshini, India approves first genome-edited rice varieties; Natura Inia News; 4 May 2025
- EU-Commission, Copernicus, Climate Change Service; Global Climate Highlights 2024